Пресс-центр / новости / Наука /
Раскрывая тайны иммунитета: TLR2 и его связь с цинком
Исследователи из Лаборатории биомолекулярной ЯМР-спектроскопии ГНЦ ИБХ РАН совместно с коллегами из Китая изучили способность Toll-подобного рецептора TLR2 связывать ионы цинка. Оказалось, что это взаимодействие происходит с высокой аффинностью и специфичностью. Toll-подобные рецепторы (TLR) играют важную роль в системе врождённого иммунитета, помогая организму распознавать патогены и запускать защитные реакции. Однако детали их работы до сих пор изучены не до конца. В новом исследовании удалось определить аминокислоты, участвующие во взаимодействии TLR2 с цинком, а также показать их важность для функционирования рецептора. Полученные данные позволяют предположить, что цинк может участвовать в регуляции активности TLR-рецепторов. Эти результаты дополняют существующие представления о механизмах работы врождённого иммунитета. Работа выполнена при поддержке гранта РНФ (№ 22-14-00020) и опубликована в FEBS Letters.
Учёные продолжают изучать, как Toll-подобные рецепторы (TLR) помогают организму распознавать инфекции и запускать иммунный ответ. Ранее исследователи обнаружили, что один из таких рецепторов, TLR1, может связывать ионы цинка с высокой аффинностью. Причём этот процесс зависит от двух аминокислот – цистеинов, один из которых играет ключевую роль в активации рецептора. Так как TLR1 работает в паре с TLR2, возник вопрос: а не взаимодействует ли и TLR2 с цинком?
Чтобы проверить эту гипотезу, учёные провели серию экспериментов. Оказалось, что TLR2 действительно способен связывать ионы цинка, причём с такой же высокой аффинностью, как и TLR1. Однако был неожиданный результат: хотя считается, что TLR1 и TLR2 взаимодействуют между собой, в проведенномэтом эксперименте они друг с другом не связывались. Вместо этого TLR2, связываясь с цинком, образовывал комплексы только с себе подобными молекулами.
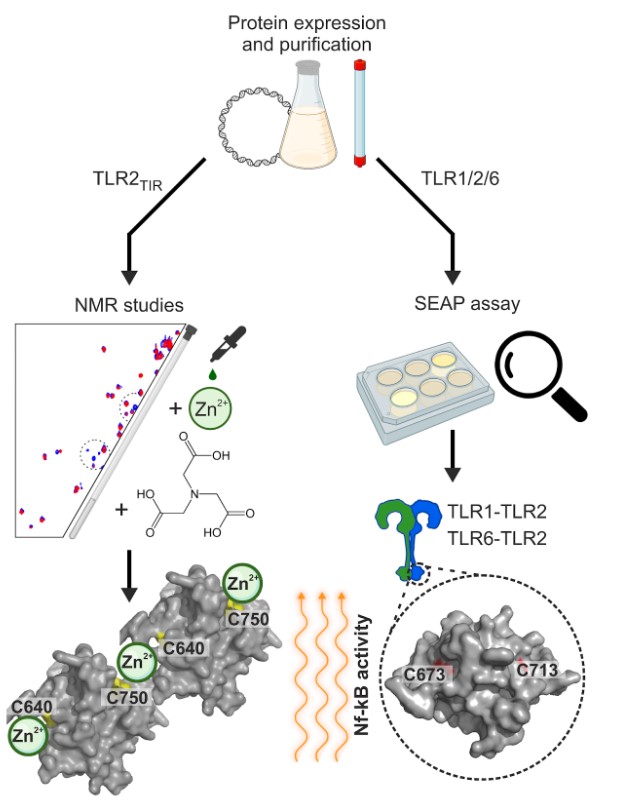
Связь между TLR2 и цинком оказалась настолько прочной, что исследователям пришлось разработать специальную методику для её измерения. Для этого они использовали хелатирующий агент NTA, который помог определить стабильность комплекса. Далее учёные решили выяснить, какие аминокислоты TLR2 отвечают за это взаимодействие. Они сосредоточились на цистеинах – именно эти остатки чаще всего участвуют в связывании этого металла. Когда все цистеины рецептора подвергались мутации, способность TLR2 связывать цинк практически исчезла. Это подтвердило, что цистеины играют ключевую роль в этом процессе. Однако попытки выделить один “главный” цистеин не увенчались успехом – оказалось, что для взаимодействия с металлом важны сразу все.
Дополнительно коллеги из Чанчуньского института прикладной химии (КНР) провели функциональные тесты. Они показали, что два из четырёх цистеинов TLR2 особенно важны для его работы: их мутации приводили к нарушению активации рецепторов.
Таким образом, это исследование дополняет существующие представления о механизмах работы TLR-рецепторов. Оно также предполагает, что цинк может участвовать в запуске иммунного ответа.
Работа выполнена при поддержке гранта РНФ № 22-14-00020 и опубликована в журнале FEBS Letters.
31 марта


